特发性肺纤维化(专业版)
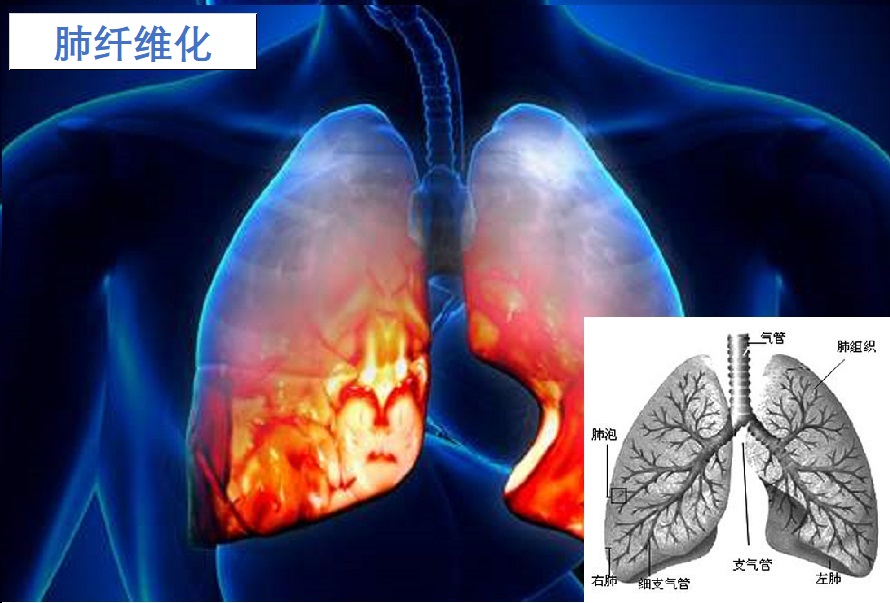
特发性肺纤维化(IPF)是一种慢性肺纤维化疾病。它引起肺部组织的炎症和纤维化(瘢痕形成、增厚),由于具体原因不明,故称为特发性。
定义
特发性肺纤维化(IPF)是一种慢性肺纤维化疾病。它引起肺部组织的炎症和纤维化(瘢痕形成、增厚),由于具体原因不明,故称为特发性。IPF可严重影响人体呼吸功能,如干咳、呼吸短促等,且病情进展、呼吸功能不断恶化。IPF死亡率高于大多数肿瘤,故又被称为“类肿瘤疾病”。病因
特发性意指IPF发病原因尚不清楚。研究人员认为,IPF是一种放大且不受控制的炎症反应,这可产生疤痕组织。但究竟什么时候开始产生是不清楚的。 随着时间的推移,疤痕环绕着肺部的薄壁气囊,使肺组织变得更厚更硬。因此,呼吸变得困难,肺部逐渐丧失将氧气传递到身体其他部位的能力。风险因素
IPF最常发生在男性,以及50岁以上的群体中。其他可能增加IPF发病的因素包括:
- 吸烟
- 肺气肿
- 病毒感染
- 职业因素,如对含有木材、金属、二氧化硅、细菌和动物蛋白质的粉尘或气溶胶喷雾、气体和烟雾等职业暴露
- 某些药物
- 胃食管反流病(GERD)
- 遗传关系,由IPF的家庭成员
症状
随着时间的推移,IPF症状会恶化,严重程度可因人而异。有的症状可能会迅速恶化(急性发作),可持续数天至数周。IPF患者逐渐开始出现部分或全部症状:
- 呼吸短暂,最初仅在身体活动期间或之后,到后来在休息时也存在。
- 干咳
- 不明原因的体重逐渐下降、消瘦
- 疲劳
- 肌肉和关节疼痛
- 指尖或有时脚趾扩大(圆柱状)
并发症
肺纤维化的并发症可能包括:- 肺动脉高压,肺动脉和毛细血管被瘢痕组织压缩,导致肺部血流阻力增加。某些形式的肺动脉高压是严重的疾病,逐渐恶化,有时是致命的。
- 右侧心力衰竭(肺心病)。
- 呼吸衰竭。
- 肺癌,长期存在的肺纤维化也会增加患肺癌的风险。
- 肺并发症,包括肺部血栓、肺部萎缩或肺部感染等
疗法
没有已知的治疗方法。治疗的目标是改善症状并延缓疾病进展,通过减少炎症和疤痕来实现。综合选项包括如下:
调整饮食与生活方式
- 健康营养,优质蛋白、深海鱼,以及丰富蔬菜、水果和坚果等。
- 不要吸烟,或戒烟
- 保持运动锻炼
- 维持健康体重
- 良好休息
营养与草本综合干预
以下是基于循证医学和循证营养学有关文献综合的结果。
有助于防控IPF的营养和草本补充剂,主要包括如下:
尽管目前的大多数证据来自实验室和动物研究,但基于目前对IPF潜在机制的理解,针对恢复氧化/抗氧化平衡和预防细胞微损伤的综合疗法,以及具有抗纤维化和抗衰老特性的综合疗法是有前景的。
1.N-乙酰半胱氨酸(NAC):
NAC可以减少氧化应激,并被用作一种强大的抗毒剂。它已被证明可以分解呼吸道粘液分泌物,使其更容易清除,因此被用于治疗与遗传性疾病囊性纤维化相关的肺纤维化1。在IPF的实验室和动物模型中,NAC已被证明可以减少氧化应激和炎症,抑制纤维化2。
对IPF患者的研究得出了相互矛盾的结果3。在一项针对服用泼尼松和硫唑嘌呤(Imuran,一种免疫抑制剂抗炎药)的IPF患者的随机对照试验中,一年内每天三次添加600mg NAC可减缓疾病进展,更好地保护肺功能,但不会显著影响死亡率4。在另一项包括155名IPF受试者的临床试验中,其中约一半接受了泼尼松、硫唑嘌呤和NAC治疗,与安慰剂相比,该组合与不良事件和死亡率增加有关5。同一研究人员发现,与安慰剂相比,单独使用NAC治疗对疾病进展没有影响,尽管NAC与更好的行走能力和生活质量有关,但这些差异在统计学上并不显著6。
基因变异可能有助于解释这些不一致的发现。研究人员发现,特定基因(人类11号染色体上的TOLLIP)内的变体可能预测对NAC治疗的反应:当临床试验的参与者根据该基因变体分组时,一种变体的参与者在接受NAC治疗时表现比安慰剂差,另一种变体对NAC疗法没有反应,而第三种变体的患者在接受NAC治疗时表现出显著改善7。希望更好地了解基因变异与药物治疗的相互作用,将有助于医生在未来进行个性化的治疗选择。
2.烟酸和牛磺酸:
烟酸(维生素B3)是烟酰胺腺嘌呤二核苷酸(NAD+)的主要前体,NAD+是与代谢和能量产生相关的细胞活动的重要辅因子。NAD+水平随着年龄的增长而降低,并与代谢功能障碍有关,而提高细胞NAD+水平已被证明可增加某些抗衰老蛋白的激活8。由于IPF与衰老密切相关9,人们认为提高NAD+水平可能是有益的。
几项使用IPF动物模型的研究结果表明,烟酸给药可以防止肺中NAD+的耗竭并减少肺纤维化10-12。对动物和肺细胞的其他研究表明,烟酸和牛磺酸的组合可能具有独特的益处。牛磺酸是一种条件必需氨基酸,已知可中和某些毒素并防止氧化性组织损伤13。来自临床前研究的证据表明,牛磺酸加烟酸可以抑制促纤维化炎症分子的活性14,15,降低肺部自由基的产生16,并最终减少肺部的胶原沉积17,18。
其他NAD+前体,如烟酰胺核糖,β-烟酰胺单核苷酸(NMN)尚未在肺纤维化的背景下进行研究。然而,一些初步证据表明,烟酰胺核苷改善了非酒精性脂肪肝小鼠模型中的肝纤维化19。
3.欧米伽3脂肪酸:
α-亚麻酸是亚麻籽和其他一些植物油中的一种必需ω-3脂肪酸。它是EPA和DHA的前体,EPA和DHA也可以从鱼油中获得。据报道,它们具有许多健康益处,主要与抗炎作用有关20。不过,α-亚麻酸转化为EPA和DHA在人体中效率低下。
在一项研究中,用鱼油代替所有膳食脂肪可以保护大鼠免受用于诱导实验性IPF样疾病的药物的侵害21。在一项研究中也观察到了类似的保护作用,在该研究中,给小鼠喂食标准实验室食物加亚麻籽油22。在另一项研究中,在暴露于相同的纤维化药物之前,接受DHA治疗的小鼠肺部和肺泡液中的炎症分子水平较低,肺纤维化较少,体重减轻较少,死亡率较低23。在另外两项研究中,用Resolvin D1或protein DX(源自DHA代谢的脂质分子)治疗已经表现出IPF样疾病的小鼠,减少了炎症和纤维化,改善了肺功能24,25。
4.脱氢表雄酮(DHEA):
DHEA是一种主要由肾上腺产生的雄性激素。DHEA及其硫酸盐形式(DHEAs)的水平随着年龄的增长而降低。低水平与慢性病和虚弱有关,高水平与健康和幸福感有关26,27。
与健康对照组相比,一些IPF患者的血液中DHEAs水平显著降低。此外,DHEA在实验室研究中抑制了肺成纤维细胞的增殖和迁移28,表明其在IPF治疗中的潜在作用。临床试验尚未调查DHEA替代疗法是否有益于IPF患者。
5.维生素D:
维生素D具有许多有益的免疫支持和抗炎作用29,30。实验动物中发现慢性维生素D缺乏会增加细胞外基质成分(如胶原蛋白)的产生,并促进肺组织纤维化31。一项有趣的研究考察了季节对肺纤维化(包括IPF)相关死亡率的影响。研究发现,与夏季相比,秋季因肺纤维化死亡的人数增加了5.2%,冬季增加了17.1%,春季增加了12.7%32。尽管季节和死亡率之间存在这种关系的原因尚不清楚,但维生素D水平较低可能是一个促成因素33。
在一项针对系统性硬化症患者的研究中,他们的血清维生素D水平低于健康对照组34。系统性硬化是一种以细胞外基质沉积和结缔组织纤维化为特征的自身免疫性疾病。在一项实验室研究中,1,25-二羟基维生素D3(维生素D的代谢活性形式)减少了人类肺上皮细胞对转化生长因子β刺激的纤维化转化35。在小鼠模型中,补充维生素D可减少博来霉素(一种有毒抗癌药物)诱导的肺纤维化36。
6.植物多酚类:
多酚是一大类植物化合物,具有强大的清除自由基和抗炎作用。多酚(包括类黄酮和酚酸)是饮食中的重要成分,并因其许多促进健康和抗衰老的特性而受到研究37,38。
许多动物和实验室研究已经检验了多酚在预防和治疗纤维化肺部疾病中的潜在作用。许多多酚在减少IPF动物模型中的纤维化、提高抗氧化酶活性和/或抑制参与IPF进展的特定炎症信号分子方面显示出了前景(尽管还需要临床试验)。其中包括:
6.1.姜黄素:
姜黄素的抗炎和清除自由基特性是众所周知的,并有助于其对包括IPF在内的肺部疾病的潜在益处39。许多临床前研究发现,在IPF动物模型中,姜黄素可以减少肺部炎症和氧化应激,并预防实验诱导的肺纤维化40-43。动物研究还表明,姜黄素可以预防肺成纤维细胞的纤维化变化44,在实验室研究中,它减少了肺泡细胞中的炎症信号传导45。
6.2.槲皮素:
槲皮素具有抗炎、清除自由基和可能的抗老化细胞特性(Senolytic)46,47。在实验室研究中,它被证明可以通过作用于一种已知与几种肺部疾病有关的分子来抑制成纤维细胞中胶原蛋白的产生48。口服槲皮素还被发现可以提高抗氧化酶水平,降低炎症标志物水平,防止氧化性肺损伤,并减少实验诱导的类似IPF的大鼠和小鼠的纤维化49,37。在一项初步研究中,槲皮素在与IPF患者的血液孵育时减少了炎性细胞因子的产生,有趣的是,健康对照受试者的血液中的抗炎作用不如IPF患者血液中明显50(Veith 2017)。
6.3.白藜芦醇:
与槲皮素一样,白藜芦醇具有抗炎和自由基复仇能力,并显示出抗癌和保护心脏的潜力。白藜芦醇已被证明可抑制受IPF影响的肺成纤维细胞的增殖和胶原产生51。白藜芦醇已被发现在IPF动物模型中对肺损伤和纤维化具有保护作用37,52。在一项研究中,白藜芦醇降低了暴露于纤维化药物的小鼠的肺组织损伤、纤维化和死亡率,还增加了Sirtuin-1的激活,这是一种可能具有重要抗纤维化功能的蛋白质53,54。
6.4.蜂胶:
咖啡酸苯乙酯是从蜂胶中提取的一种黄酮类化合物,具有调节免疫功能和抗炎等多种生物活性。研究表明,咖啡酸苯乙酯可以防止实验诱导的IPF样条件下动物肺部的胶原沉积。在该IPF动物模型中,还发现它降低了肺和血浆中关键的促纤维化和炎症分子的水平55,56,并减少了肺组织自由基57。蜂胶治疗还抑制了由IPF相关炎症分子触发的人类肺泡细胞中的促纤维化信号传导58。
6.5.其他:
包括绿茶多酚EGCG59、葡萄籽提取物原花青素60以及柑橘类黄酮61等。
更多可查看其个性化综合干预方案如下:
- 支持肺健康:
- 肺纤维化管理:
医疗干预
一般治疗措施包括如下:
药物治疗是主要的方式,但它并不适合所有人:
- 减少炎症
- 抑制免疫反应
- 减缓纤维化的进展
晚期IPF患者,如果对其他治疗没有反应,可考虑肺移植。
支持性护理
- 有些人可能需要接受氧气。这将有助于他们呼吸。
- 可能需要肺康复计划来改善肺功能。
- 营养支持。
- 获取适当的疫苗以预防肺部感染,包括每年注射流感疫苗和肺炎疫苗。
- 调整生活方式有助减缓疾病:
- 不吸烟
- 吃健康的饮食
- 定期进行锻炼
- 注意及时休息
预防
没有可靠的方法来预防IPF。在某些职业中避免吸烟和戴口罩可能会有所帮助。
参考文献:
1. Rushworth GF et al. Existing and potential therapeutic uses for N-acetylcysteine: the need for conversion to intracellular glutathione for antioxidant benefits. Pharmacology & therapeutics. Feb 2014;141(2):150-159.
2. Myllarniemi M et al. Pharmacological treatment of idiopathic pulmonary fibrosis - preclinical and clinical studies of pirfenidone, nintedanib, and N-acetylcysteine. Eur Clin Respir J. 2015 Feb 10:2
3. Sun T et al. Efficacy of N-Acetylcysteine in Idiopathic Pulmonary Fibrosis: A Systematic Review and Meta-Analysis. Medicine. May 2016;95(19):e3629.
4. Demedts M et al. High-dose acetylcysteine in idiopathic pulmonary fibrosis. N Engl J Med. Nov 24 2005;353(21):2229-2242.
5. Raghu G et al. Prednisone, azathioprine, and N-acetylcysteine for pulmonary fibrosis. N Engl J Med. May 24 2012;366(21):1968-1977.
6. Martinez FJ et al. Randomized trial of acetylcysteine in idiopathic pulmonary fibrosis. N Engl J Med. May 29 2014;370(22):2093-2101.
7. Oldham JM et al. Pharmacogenetics and interstitial lung disease. Current opinion in pulmonary medicine. Sep 2016;22(5):456-465.
8. Srivastava S. Emerging therapeutic roles for NAD(+) metabolism in mitochondrial and age-related disorders. Clin Transl Med. Dec 2016;5(1):25.
9. Sgalla G et al. Idiopathic pulmonary fibrosis: pathogenesis and management. Respiratory research. Feb 22 2018;19(1):32.
10. Wang QJ et al. Niacin attenuates bleomycin-induced lung fibrosis in the hamster. Journal of biochemical toxicology. Spring 1990;5(1):13-22.
11. Nagai A et al. Effects of nicotinamide and niacin on bleomycin-induced acute injury and subsequent fibrosis in hamster lungs. Experimental lung research. Jul-Aug 1994;20(4):263-281.
12. O'Neill CA et al. Biochemical mechanisms for the attenuation of bleomycin-induced lung fibrosis by treatment with niacin in hamsters: the role of NAD and ATP. Experimental lung research. Jan-Feb 1994;20(1):41-56.
13. AMR. Taurine - monograph. Alternative medicine review: a journal of clinical therapeutic. Feb 2001;6(1):78-82.
14. Gurujeyalakshmi G et al. Taurine and niacin block lung injury and fibrosis by down-regulating bleomycin-induced activation of transcription nuclear factor-kappaB in mice. The Journal of pharmacology and experimental therapeutics. Apr 2000b;293(1):82-90.
15. Gurujeyalakshmi G et al. Regulation of transforming growth factor-beta1 mRNA expression by taurine and niacin in the bleomycin hamster model of lung fibrosis. American journal of respiratory cell and molecular biology. Mar 1998;18(3):334-342.
16. Gurujeyalakshmi G et al. Suppression of bleomycin-induced nitric oxide production in mice by taurine and niacin. Nitric Oxide. Aug 2000a;4(4):399-411.
17. Blaisdell RJ et al. Dietary supplementation with taurine and niacin prevents the increase in lung collagen cross-links in the multidose bleomycin hamster model of pulmonary fibrosis. Journal of biochemical toxicology. Apr 1994;9(2):79-86.
18. Giri SN et al. Amelioration of bleomycin-induced lung fibrosis in hamsters by dietary supplementation with taurine and niacin: biochemical mechanisms. Environ Health Perspect. Dec 1994;102 Suppl 10:137-147.
19. Zhou CC et al. Hepatic NAD(+) deficiency as a therapeutic target for non-alcoholic fatty liver disease in ageing. British journal of pharmacology. Aug 2016;173(15):2352-2368.
20. Baker EJ et al. Metabolism and functional effects of plant-derived omega-3 fatty acids in humans. Progress in lipid research. Oct 2016;64:30-56.
21. Kennedy JI et al. Dietary fish oil inhibits bleomycin-induced pulmonary fibrosis in the rat. Experimental lung research. Mar 1989;15(2):315-329.
22. Lawrenz J et al. Dietary Flaxseed Oil Protects against Bleomycin-Induced Pulmonary Fibrosis in Rats. Pulmonary medicine. 2012;2012:457031.
23. Yatomi M et al. 17(R)-resolvin D1 ameliorates bleomycin-induced pulmonary fibrosis in mice. Physiological reports. Dec 2015;3(12).
24. Li H et al. Posttreatment with Protectin DX ameliorates bleomycin-induced pulmonary fibrosis and lung dysfunction in mice. Sci Rep. May 3 2017;7:46754.
25. Lois K et al. Adrenal Androgens and Aging. In: De Groot LJ, Chrousos G, Dungan K, et al., eds. Endotext. South Dartmouth (MA): MDText.com, Inc.; 2000.
26. Samaras N et al. Off-label use of hormones as an antiaging strategy: a review. Clin Interv Aging. 2014;9:1175-1186.
27. Mendoza-Milla C et al. Dehydroepiandrosterone has strong antifibrotic effects and is decreased in idiopathic pulmonary fibrosis. The European respiratory journal. Nov 2013;42(5):1309-1321.
28. Yin K et al. Vitamin D and inflammatory diseases. Journal of inflammation research. 2014;7:69-87.
29. Hoe E et al. Anti-Inflammatory Effects of Vitamin D on Human Immune Cells in the Context of Bacterial Infection. Nutrients. Dec 12 2016;8(12).
30. Shi Y et al. Chronic vitamin D deficiency induces lung fibrosis through activation of the renin-angiotensin system. Sci Rep. Jun 12 2017;7(1):3312.
31. Olson AL et al. Seasonal Variation: Mortality From Pulmonary Fibrosis Is Greatest in the Winter. Chest. Jul 2009;136(1):16-22.
32. Grant WB et al. Seasonal variations of U.S. mortality rates: Roles of solar ultraviolet-B doses, vitamin D, gene exp ression, and infections. The Journal of steroid biochemistry and molecular biology. Oct 2017;173:5-12.
33. Zhang L et al. Association between the serum level of vitamin D and systemic sclerosis in a Chinese population: a case control study. International journal of rheumatic diseases. Aug 2017;20(8):1002-1008.
34. Jiang F et al. 1α,25-dihydroxyvitamin D3 Attenuates TGF-β-Induced Pro-Fibrotic Effects in Human Lung Epithelial Cells through Inhibition of Epithelial–Mesenchymal Transition. Nutrients. 2017;9(9):980.
35. Zhang Z et al Preventive effects of vitamin D treatment on bleomycin-induced pulmonary fibrosis. Sci Rep. Dec 2 2015;5:17638.
36. Impellizzeri D et al. Protective effect of polyphenols in an inflammatory process associated with experimental pulmonary fibrosis in mice. The British journal of nutrition. Sep 28 2015;114(6):853-865.
37. Queen BL et al. Polyphenols and aging. Current aging science. Feb 2010;3(1):34-42.
38. Lelli D et al. Curcumin use in pulmonary diseases: State of the art and future perspectives. Pharmacological research: the official journal of the Italian Pharmacological Society. Jan 2017;115:133-148.
39. Punithavathi D et al. Curcumin inhibition of bleomycin-induced pulmonary fibrosis in rats. British journal of pharmacology. Sep 2000;131(2):169-172.
40. Xu M et al. Effects of curcumin in treatment of experimental pulmonary fibrosis: a comparison with hydrocortisone. Journal of ethnopharmacology. Jun 13 2007;112(2):292-299.
41. Zhao CJ et al. [Effects of curcumin on bleomycin-induced damages in pulmonary functions in rats]. Zhongguo Zhong yao za zhi. Jun 2008;33(12):1434-1438.
42. Smith MR et al. Curcumin inhibits fibrosis-related effects in IPF fibroblasts and in mice following bleomycin-induced lung injury. American journal of physiology. Lung cellular and molecular physiology. May 2010;298(5):L616-625.
43. Liu D et al. Curcumin Inhibits Transforming Growth Factor beta Induced Differentiation of Mouse Lung Fibroblasts to Myofibroblasts. Frontiers in pharmacology. 2016;7:419.
44. Gouda MM et al. Curcumin alleviates IL-17A-mediated p53-PAI-1 expression in bleomycin-induced alveolar basal epithelial cells. Journal of cellular biochemistry. Feb 2018;119(2):2222-2230.
45. Anand David AV et al. Overviews of Biological Importance of Quercetin: A Bioactive Flavonoid. Pharmacognosy reviews. Jul-Dec 2016;10(20):84-89.
46. Zhu Y et al. The Achilles' heel of senescent cells: from transcriptome to senolytic drugs. Aging Cell. Aug 2015;14(4):644-658.
47. Nakamura T et al. Attenuation of transforming growth factor-beta-stimulated collagen production in fibroblasts by quercetin-induced heme oxygenase-1. American journal of respiratory cell and molecular biology. May 2011;44(5):614-620.
48. Verma R et al. Evaluating the Ameliorative Potential of Quercetin against the Bleomycin-Induced Pulmonary Fibrosis in Wistar Rats. Pulmonary medicine. 2013;2013:921724.
49. Veith C et al. The disturbed redox-balance in pulmonary fibrosis is modulated by the plant flavonoid quercetin. Toxicology and applied pharmacology. Dec 1 2017;336:40-48.
50. Fagone E et al. Resveratrol inhibits transforming growth factor-beta-induced proliferation and differentiation of ex vivo human lung fibroblasts into myofibroblasts through ERK/Akt inhibition and PTEN restoration. Experimental lung research. Apr 2011;37(3):162-174.
51. Akgedik R et al. Effect of resveratrol on treatment of bleomycin-induced pulmonary fibrosis in rats. Inflammation. Oct 2012;35(5):1732-1741.
52. Rong L et al. Sirt 1 activator attenuates the bleomycin-induced lung fibrosis in mice via inhibiting epithelial-to-mesenchymal transition (EMT). European review for medical and pharmacological sciences. May 2016;20(10):2144-2150.
53. Zeng Z et al. Activation and overexpression of Sirt1 attenuates lung fibrosis via P300. Biochemical and biophysical research communications. May 13 2017;486(4):1021-1026.
54. Larki-Harchegani A et al. Evaluation of the Effects of Caffeic Acid Phenethyl Ester on Prostaglandin E2 and Two Key Cytokines Involved in Bleomycin-induced Pulmonary Fibrosis. Iranian journal of basic medical sciences. Jul 2013;16(7):850-857.
55. Larki A et al. Regulatory effect of caffeic acid phenethyl ester on type I collagen and interferon-gamma in bleomycin-induced pulmonary fibrosis in rat. Res Pharm Sci. Oct 2013;8(4):243-252.
56. Ozyurt H et al. Inhibitory effect of caffeic acid phenethyl ester on bleomycine-induced lung fibrosis in rats. Clinica chimica acta; international journal of clinical chemistry. Jan 2004;339(1-2):65-75.
57. Kao HF et al. Propolis inhibits TGF-beta1-induced epithelial-mesenchymal transition in human alveolar epithelial cells via PPARgamma activation. International immunopharmacology. Mar 2013;15(3):565-574.
58. Sriram N et al. Epigallocatechin-3-gallate augments antioxidant activities and inhibits inflammation during bleomycin-induced experimental pulmonary fibrosis through Nrf2-Keap1 signaling. Pulmonary pharmacology & therapeutics. Jun 2009;22(3):221-236.
59. Agackiran Y et al. The efficiency of proanthocyanidin in an experimental pulmonary fibrosis model: comparison with taurine. Inflammation. Aug 2012;35(4):1402-1410.
60. Zhou XM et al. Inhibitory effects of citrus extracts on the experimental pulmonary fibrosis. Journal of ethnopharmacology. Oct 29 2009;126(1):143-148.
参考来源:
美国梅奥诊所
www.mayoclinic.org
美国肺纤维化基金会
https://www.pulmonaryfibrosis.org/
美国肺脏协会
http://www.lung.org
美国肺纤维化联盟网
http://www.coalitionforpf.org
加拿大肺脏协会
http://www.lung.ca
免责声明和安全信息
- 本信息(包括任何附带资料)不是为了取代医生或有关合格从业人士的建议或忠告。
- 任何人如果想要对本文涉及的药物、饮食、运动或其他生活方式的使用、或改变调整,以预防或治疗某一特定健康状况或疾病,应首先咨询医生或有关合格从业人士,并获得他/她们的许可。妊娠和哺乳妇女在使用本网站任何内容前,尤其应征求医生的意见。
- 除非另有说明,本网站所述内容仅适用于成人。
- 本网站所推荐的任何产品,消费者应该以实际的产品标签内容为准,尤其应关注重要的安全信息以及产品最新信息,包括剂量、使用方法和禁忌症等。
- 由于循证医学研究、文献及有关产品处于不断的变化中,本网站工作人员将尽力更新。
- 本网站不能保证所载文章内容、综合干预方案以及相关成分或产品述及的健康益处,也不承担任何责任。

